| 인슐린 저항성의 검사 및 클램프 연구 |
|
이혜진
이화여자대학교 의학전문대학원 |
|
인슐린저항성은 대사질환 발현에 주된 위험요인이며, 유전적, 환경적 영향을 받는다. 인슐린 저항성의 정량적 검사는 인슐린 저항성의 유무, 중증도를 파악하는데 있어 유용하나, 임상에서 흔히 시행되고 있지 않으며, 주로 연구 목적으로 사용되고 있다.
인슐린 저항성의 평가 방법은 dynamic test 와 simple index로 나뉠 수 있다 (표 1) (1). 연구자가 시행하는 연구의 목적에 따라 인슐린 저항성의 평가 방법이 선택될 수 있으며 (그림 1) (2), 연구 대상수, 대상군의 glycemic status, 재원, 장비, 인력 등이 인슐린 저항성 측정 방법 선택에 중요한 변수로 작용할 수 있다. 1. Dynamic Test 1) Hyperinsulinemic euglycemic clamp test Hyperinsulinemic euglycemic clamp test 는 인슐린 저항성 평가의 gold standard 로 여겨지고 있다. 이 검사는 일정량의 인슐린을 정맥 주사하여 인위적인 고인슐린 상태를 유발하고, 일정한 혈당을 유지시키기 위하여 포도당 주입량을 조절하는 것을 그 기본으로 한다 (3). 검사를 위하여 팔에 정맥관을 삽입하여 포도당과 인슐린 농도 측정을 위한 혈액을 채취하는데, 동맥화된 정맥혈 채취를 위하여 heating pad를 팔에 두는 것이 좋다. 인슐린을 일정한 속도로 주입하면서, 포도당 농도를 매 5~10분마다 측정하여 20% 포도당 용액의 주입속도를 조정함으로써, 혈증 포도당 농도를 일정하게 (80-90 mg/dl) 유지하게 된다. 일정한 포도당 농도가 유지될 때, glucose infusion rates (GIR)은 glucose disposal rate (M)과 같게 되며, 이는 약 2-3시간 동안 진행되는 clamp test의 마지막 30분 동안에 주입되는 포도당의 평균속도로 나타나다. M value 는 mg/kg body weight/min 으로 표시한다 (protocol 1). 2) Minimal model analysis of frequently sampled intravenous glucose tolerance test (FSIVGTT) Hyperinsulinemic euglycemic clamp test 의 복잡성 때문에 FSIVGTT 가 silver standard 로 제안되고 있다. FSIVGTT는 포도당 bolus 주입 전후 혈당과 인슐린 농도에 대한 data를 가지고 간접적으로 인슐린 저항성을 평가한다. 인슐린 감수성 지수 (Si) 평가를 위하여는 minimal model analysis가 필요하며, MINMOD 같은 software package를 사용할 수 있다. MINMOD program은 Si 뿐 아니라 glucose effectiveness (Sg), βcell activity (β-cell), acute insulin response (AIR), disposition index (DI), area under the curve (AUC)등을 계산할 수 있다 (4, 5)(protocol 2). 2. Simple indices of insulin resistance 1) Oral glucose tolerance test (GTT)-derived indices 경구 당부하검사를 통하여 포도당, 인슐린 농도를 측정하여 다양한 인슐린저항성 변수를 계산할 수 있다. Dynamic technique이 사용될 수 없을 때, GTT-derived index가 인슐린 저항성을 측정하는 대안이 될 수 있으며, 그 종류는 다음 표와 같다 (표 2) 2) Fasting sample-derived indices 가장 흔히 사용되는 인슐린저항성의 지표는 공복 인슐린 농도와 혈당을 이용한 계산식이다. 이 방법은 간단하고, 저렴해서 광범위하게 사용되고 있으며 다음과 같은 종류가 있다 (표 3). 다양한 종류의 인슐린 저항성 측정법이 있으며, 연구자가 의도하는 바에 따라 적적한 인슐린 저항성 측정법을 선택할 수 있겠다.    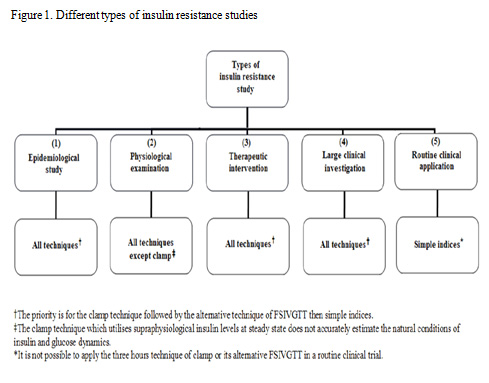 PROTOCOL 1. Euglycemic Hyperinsulinemic Clamp test Protocol Euglycemic hyperinsulinemic pump Ask subject - To avoid unusual physical exercise, alcohol consumption or any major change in caloric intake during the 2 days preceding the day of exam - To avoid food intake from midnight the preceding day and avoid any medication, smoking - allow drinking water in the morning Before exam - Empty bladder - Measure BW, BP, PR - insert polyethylene catheter in the brachial vein in the left and right arms both arms placed on heating pads to obtain arterialized blood - 12 mL albumin (200 mg/mL) added to 487mL N/S add 40 U insulin (rapid, 40U/ml) and flush the tube to saturate the walls with insulin - add K(20 mmol) to 1L of 20% glucose Baseline blood sample for glucose -> insulin and glucose infusion insulin priming : 2mU/min/kg for 20min -> 1mU/min/kg for 120min glucose infusion : 20ml/h 로 시작 target whole blood glucose : 90 mg/dl blood sample every 5 min to adjust glucose infusion rate at the end : blood sample for determination of plasma insulin calculation of insulin sensitivity - GIR per min adjust for BW or for fat-free mass for each 20-min interval during the final hours of the 2h exam 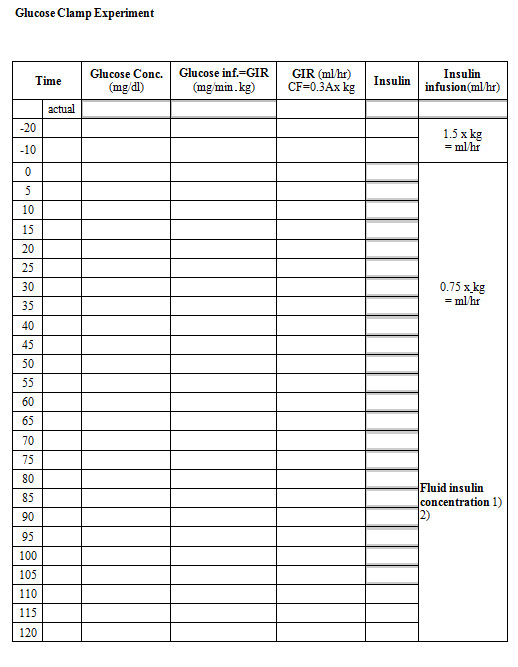 PROTOCOL 2. FSIVGTT Protocol 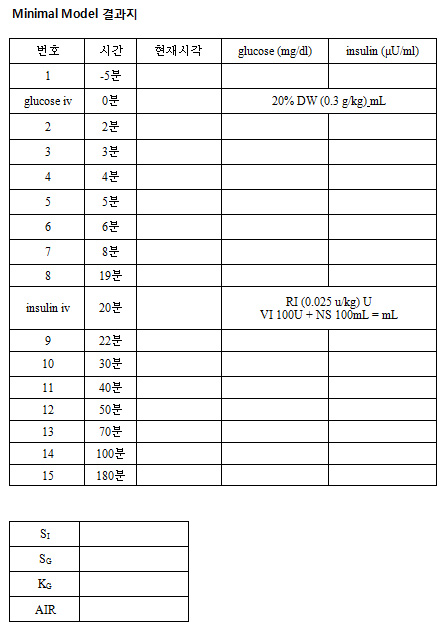 References
|